Klinische Studien

Klinische Studien sind Teil unserer Mission, innovative Arzneimittel zu entwickeln und weltweit bereitzustellen. Bei diesen klinischen Studien, die nur möglich sind, weil (gesunde und erkrankte) freiwillige Testpersonen sich zu einer Teilnahme bereit erklären, folgen wir bester Praxis in Bezug auf Sicherheit und Transparenz.
Medikamente retten und verändern das Leben von Menschen, doch der Prozess der Entwicklung und Zulassung eines Medikaments ist langwierig, komplex, unterliegt strengen Auflagen und dauert mehrere Jahre. Zunächst, in der sogenannten präklinischen Phase, werden die Medikamente im Labor untersucht und wenn die ersten Ergebnisse vielversprechend sind, werden die experimentellen Medikamente strengen Tests unterzogen, um festzustellen, ob sie effektiv wirken, stabil, reproduzierbar und zuverlässig sind. Diese Tests können unter Verwendung von Computersimulationen, mit Zellen und/oder Tieren (falls unbedingt erforderlich) durchgeführt werden. Wenn diese Phase erfolgreich durchgeführt wurde, wandeln wir die experimentellen Medikamente in sichere und robuste Medikamente um, die in klinischen Studien verwendet und mit großer Vorsicht an Menschen getestet werden. Klinische Studien zielen darauf ab zu verstehen, ob das Medikament bei der Behandlung oder Prävention der Erkrankung, für die es entwickelt wurde, sicher und wirksam ist, ob es bessere Ergebnisse erzielt als die bereits verfügbaren Therapien und ob es die Lebensqualität der Erkrankten verbessert. Die Zulassung eines Medikaments durch die Zulassungsbehörden und sein Markteintritt hängen von der Vorlage eines wissenschaftlichen Dossiers ab, dessen wesentlicher Bestandteil die Ergebnisse klinischer Studien sind.
Die Phasen klinischer Studien
Klinische Studien werden sorgfältig konzipiert, überprüft und geplant und müssen vor Beginn von Behörden und Ethikkommissionen genehmigt werden. Teilnehmen können Menschen jeden Alters nach zuvor festgelegten Teilnahmekriterien.
Klinische Studien werden in 4 Phasen unterteilt:
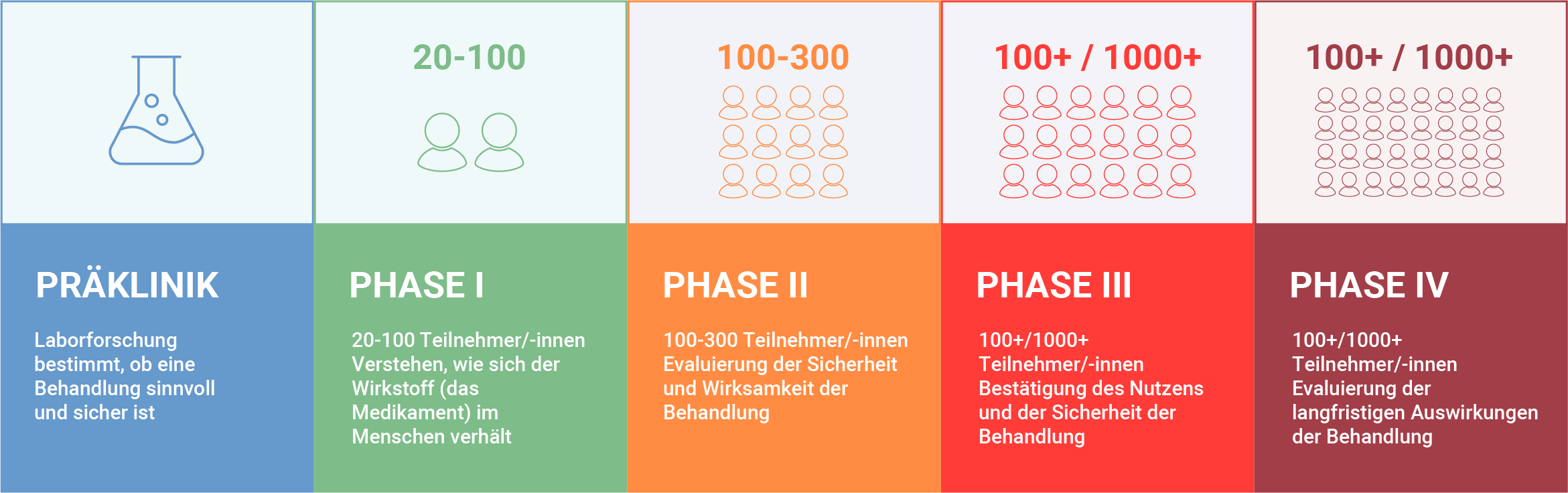
Phase I
20-100 gesunde freiwillige TestpersonenIn dieser Phase besteht das Ziel darin, die Sicherheit des Arzneimittels zu bewerten und seine Nebenwirkungen kennenzulernen. Wir versuchen zu verstehen, wie das Arzneimittel im menschlichen Körper wirkt und welche Dosis in den folgenden Phasen angemessen ist. Diese Phase ist kurz und die freiwillige Testpersonen werden im Forschungszentrum, in dem die Studie durchgeführt wird, engmaschig betreut.








